Радикалы органических кислот: ацетат — (уксусная кислота), пируват — (пировиноградная кислота), лактат — (молочная кислота), бета-гидроксибутират — (бета-гидроксимасляная кислота), ацетоацетат — (ацетоуксусная кислота).
Главная страница ● Основные положения ● Электролиты
глава 1.2.1.
Общие данные
Под электролитами понимают соли, кислоты, основания, которые в водном растворе в
большей или меньшей степени распадаются (диссоциируют) на свободные подвижные
ионы.
Натрий и хлор, например, находятся в кристалле поваренной соли также в виде
ионов, но связанных ионной решеткой. В процессе растворения она вследствие
диссоциации становится подвижной, и решетчатая структура разрывается молекулами
воды.
Ионы представляют собой электрически заряженные частицы, которые при
диссоциации электролитов становятся подвижными в водном растворе, их соединению
препятствуют молекулы воды.
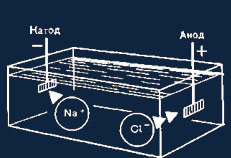
Добавим, например, поваренную соль в воду,— ионы натрия и хлора станут
подвижными. В поле постоянного тока (рис. 3) положительно заряженные частицы
двигаются катоду (катионы), отрицательно заряженные — к аноду (анионы).
Валентность соответствует значению положительного или отрицательного заряда.
Основные катионы, находящиеся в организме:
натрий Na+
калий К+
кальций Са2+
магний Mg2+
Основные анионы, находящиеся в организме:
хлор С1—
гидрокарбонат НСО3—
фосфат Н2РО4—; НРО42—
сульфат SО42—
белки
Рис. 3. Движение катионов и анионов в поле постоянного тока.

Радикалы органических кислот: ацетат — (уксусная кислота), пируват —
(пировиноградная кислота), лактат — (молочная кислота), бета-гидроксибутират —
(бета-гидроксимасляная кислота), ацетоацетат — (ацетоуксусная кислота).
|
● |
● |
● |
● |
● |
● |
● |
● |
copyright©surgerycom